
今天Sage宣布其GABA受体阳性调控剂Sage217(又名Zuranolone)在一个叫做Mountain的三期临床失败。这个试验招募581位重症抑郁(MDD)患者,
Continue reading …
今天Aurinia宣布其环孢素衍生物voclosporin在一个增生性狼疮肾炎(LN)三期临床达到所有一级、二级终点。这个叫做AURORA的试验招募357位LN患者,在霉酚酸酯和低剂量甾体激素背景上分别使用voclosporin和安慰剂,一级终点位52周肾应答率。
Continue reading …
今天Incyte宣布FDA接受了其FGFR抑制剂pemigatinib在FGFR2融合或易位晚期胆管癌二线以后治疗的上市申请。在一个叫做FIGHT-202的二期临床试验中pemigatinib在这个人群产生36%应答率、中位应答时间为7.5个月。
Continue reading …
今天麻省总医院和哈佛大学科学家在《Cell Reports》发表一项工作,评价老药色甘酸钠在SOD1变异(G93A)驱动小鼠ALS模型的疗效。作者发现腹腔注射色甘酸钠可以显著推迟ALS症状出现(20小鼠天,相当于人的10年)、增加小鼠肌肉功能(根据一个叫做PaGE 的指标)、并延长雌性小鼠寿命(但对雄性无影响)。表征上色甘酸钠缓解肌肉去神经、改善运动神经元生存、并降低炎症细胞因子水平。
Continue reading …
今天FDA批准了Global Blood Therapeutics, Inc. (GBT)的小分子镰刀细胞疾病(SCD)药物Oxbryta (通用名voxeloto,曾用名GBT440) 用于12岁以上患者的治疗。
Continue reading …
今天在亚洲ESMO年会上加拿大生物技术公司Zymeworks与合作伙伴百济神州公布了其HER2双特异抗体ZW25的一个晚期实体瘤一期临床结果。这个试验招募69位晚期HER2表达非乳腺癌实体瘤患者
Continue reading …
Alnylam的Givosiran(商品名Givlaari)今天被FDA批准用于一种叫做急性肝卟啉病(AHP)的超级罕见病,成为第二个在美国上市的RNAi药物。这个批准是根据一个叫做ENVISION的三期临床试验,
Continue reading …
今天Bloomberg News报道诺华可能收购开发PCSK9 RNAi药物inclisiran的Medicines Company,令今天MDCO股票上扬20%。
Continue reading …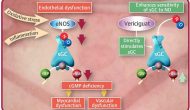
今天默沙东与合作伙伴拜耳宣布其心衰药物、可溶性鸟苷酸环化酶(sGC)激动剂Vericiguat在一个叫做VICTORIA的国际多中心三期临床试验达到由心衰住院和心血管死亡组成的复合一级终点。
Continue reading …
昨天FDA专家组以16:0全票支持将Amarin的纯EPA鱼油制剂Vascepa标签扩展到心血管预防,矿物油作为安慰剂并未令专家组质疑关键试验Reduce-it结果的可靠性,但专家对是否将标签限制在二级预防、出血和心率不齐危险等进行了讨论。
Continue reading …
今天FDA通过加速审批通道批准了百济神州的BTK抑制剂Brukinsa (通用名zanubrutinib)用于治疗至少失败一种疗法的套细胞淋巴瘤。这个审批是根据一个86人参与的单臂临床试验结果,Brukinsa在这个人群的应答率为84%、中值应答时间为19.5个月。
Continue reading …
今天在SITC年会上匹斯堡大学的Kirkwood教授汇报了Checkmate Pharmaceutical的TLR9激动剂CMP-001单方或与K药组合在K药耐药恶黑患者的一个二期临床结果。
Continue reading …
今天百健宣布扩大与韩国生物技术药企业三星生物的合作,以1亿美元首付、2.1亿美元里程金获得视网膜疾病药物雷珠单抗(商品名Lucentis)和阿柏西普(商品名Eylea) 生物类似药(分别叫做SB11、SB15)在欧美、日本等几个主要 市场的权益。同时百健还将获得二者合作的三个TNF药物在中国市场的权益。两个公司的联合公司Samsung Bioepis将负责这两个药物的临床开发。
Continue reading …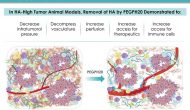
今天美国生物技术公司Halozyme宣布其透明质酸酶制剂PEGPH20在一个叫做HALO-301的胰腺癌三期临床失败。这个试验在吉西他滨和ABRAXANE®背景上比较PEGPH20与安慰剂作为晚期胰腺癌一线药物对OS的影响,
Continue reading …





















 微信号:美中药源
微信号:美中药源