从基因的角度解析心血管疾病风险(五)精准医学与营养学
By 沈骊 GB HealthWatch

第五章:精准医学和营养学
精准医学和营养学的要义在于有的方矢,在基因检测的基础上把疾病预防提到最早最有针对性。从生物学的角度可以这么描述:我们所有的人生下来都会患上一个共同的疾病,这个病就是动脉粥样硬化。没有一个人能够逃脱,只是这个病的病程很长,从出生就开始,早期隐避没有症状;极少数基因组合特别差又没有极早诊断治疗的人,50岁以前可能发病,突发心肌梗塞或脑卒中;大多数人会在50岁到90岁之间陆续发病;在现实的医疗条件下,一小部分有极佳基因组合的人可能把发病时间推迟到120岁。目前还没有任何药物可以逆转动脉粥样硬化,但是可能减缓进程;如果精准医学和营养学得到充分的发展和应用,让诊断预防和治疗一条龙执行得早执行得精准恰当,是有可能帮助大多数人在现有的平均寿命基础上更健康的多活20年,让100岁成为常态。

图1. 精准时代分子营养学原理完全整合到数字化的生活中,在不知不觉间达到最佳的疾病预防效果。
我们在前面四章中分别介绍了动脉粥样硬化的分子生物学基础和病理过程。我们可以清晰的看到,只要身体的各器官组织需要用胆固醇构建细胞膜,合成负责身体每天运着的甾体激素,只要胆固醇供应链依赖血液循环搞运输,只要人还活着心脏在跳血液在流动,我们就没有人能够逃避动脉粥样硬化的命运。动脉粥样硬化的程度与年龄成正比,与血液中胆固醇的浓度成正比,与高血压成呈正相关,与吸烟呈正相关,与男性性别呈正相关。更准确的说,与这些因素的终生累积剂量呈正比,可以简化的表示为,终生累积剂量=(年龄X浓度)。这样,假设一个人携带有家族性高胆固醇症基因突变,从小胆固醇就很高在190mg/dL水平,那么这个人在40岁的时候血管内壁所面对过的胆固醇累积总剂量就相当于一个正常人(假设胆固醇是100mg/dL) 在76岁所面对过的累积总剂量。这就难怪那些有高胆固醇血症基因突变的病人如果没有及早实施降胆固醇治疗,男的55岁以前女在60岁以前发生心肌梗塞事件的几率是普通人的13-20倍。而如果有这些突变的人被早期诊断,从青少年时期起就开始釆用降胆固醇药物和饮食治疗,临床跟踪实验结果证实这些人的心血管病症状出现的时间会推迟15-20年。除了胆固醇以外,其他的风险和保护因素也多半是以终生累积总剂量的方式加快或减缓动脉粥样硬化的进程。
分子营养学-如何减缓动脉粥样硬化的进程
在讨论下面内容前作者特此申明,作者本人既不是执照医生,也不是执照营养师,作者是专注于基因营养学研究的分子生物学家。以下内容旨在为读者解析基本概念,讨论可实施方法的分子生物学基础,不应作为医学推荐使用。
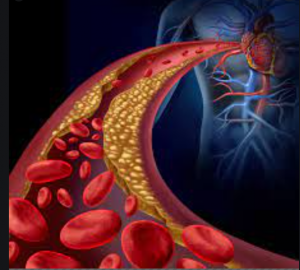
图2. 动脉粥样硬化
在第三章我们详细介绍过动脉粥样硬化的形成过程,包括动脉血管壁的损伤,血流动力学的影响,脂蛋白微粒和胆固醇沉积,免疫细胞吞噬和泡沫细胞形成,炎症反应和钙化,以及胆固醇反转运清扫过程。这一章我们将按同样的步骤来分析如何才能最大程度减缓动脉粥样硬化的进程。
控制高血压
动脉粥样化病灶的起始点是动脉血管壁的某些位置出现破损,破损的出现与血压和血管转弯分岔处的血流动力学有关。我们没法让血管不转弯不分岔,我们可以做到的是避免高血压。但是血压不可能降得太低,只要人活着血液要流动,破损总是会出现的,只是把机率降小一些,减少血管壁上的病灶数目。从基因的角度看并没有发现人群中有人携带血压调控相关变异造成心血管病风险严重增加,观察到的最大遗传风险变异发生在NOS3和GUCY1A1基因上,这两个基因都是调节血管壁平滑肌的紧张度,并不直接控制血压。为什么没有高血压突变大力增加动脉粥样硬化,作者认为人体对血压大幅升高和降低的容忍度很底,那此会造成大幅血压变化的变异不被允许在进化过程中保留下来。大多数人是年纪大了以后动脉粥样硬化造成血管狭窄才开始血压升高。临时紧张激动也会造成高血压,突然血压升高也会造成对血管壁的损伤,有时还会是触发心肌梗塞或者脑卒中的诱因。降低钠摄入量,增加钾摄入量和适度的体育锻练都可以帮助降低血压。很大一部分中国人携带一个ADD1基因的变异,这个基因在肾脏协助钠离子回收,有这个基因变异的人对盐特别敏感,多吃一点盐会明显增高血压。在饮食方面,对中国人要特别担心不咸酱油,有的酱油为了吃起来不咸用的是尝不出咸味的钠盐,一小勺酱油的钠含量有900mg左右。高钾食品和利尿食品有利于降血压。高钾食品包括各种豆子,根茎类和绿叶蔬菜,土豆红薯南瓜四季豆菠菜是最常见的例子。当饮食和运动不足以维持良好的血压时,药物治疗就一定要开始,并且需要每天坚持终身服药。
降低胆固醇
一但血管壁损伤已经出现,血液中流动的低密度脂蛋白微粒LDL的数量,大小以及它所运载的胆固醇的多少就会很大程度决定每一个病灶的含油量和恶化程度。LDL微粒数量越多,个头越少,问题就越坏,因此也不单单是胆固醇量的问题。降胆固醇,把胆固醇降到身体能容忍的最低量是目前医学界对有高风险人群的推荐治疗。有数据估计,每降低1mg/dL 低密度胆固醇LDL-C,可以得到2%降低心血管疾病死亡率的收益。对于那些携带有家族性高胆固醇血症基因突变的人来说,在青少年时期就应该考虑降胆固醇药物和饮食治疗。对那些没有严重基因突变但胆固醇水平偏高的人,可以先尝试饮食控制,如果胆固醇仍达不到理想水平(100mg/dL),就应该考虑药物治疗。同样,胆固醇水平也不可能降得无限低,如果胆固醇供运不足会使所有的甾体激素合成不足,这包括所有的性激素和肾上腺皮质激素,其结果是精力差性欲低下,皮肤不保水易感染。另外胆固醇降得太低的另一个副作用是增加二型糖尿病风险。食品对胆固醇浓度影响最大的是油脂,特别是饱和脂肪酸,高油脂饮食可能使空腹LDL-C水平增加20-30%。相反,在没有APOE基因缺陷的情况下,适量摄入高胆固醇食品,例如吃两个鸡蛋黄对空腹LDL-C的浓度并无影响。这是因为脂肪酸是肝脏自主合成胆固醇的更好底物,而食品中摄入的胆固醇会抑制肝脏合成。过度摄入胆固醇也是不对的,例如每天吃10个鸡蛋的减肥餐,过多的胆固醇进入肝脏也会被肝脏贮存和再分泌到血液中。有APOE基因某些变异的人,包括APOE2/E2纯合子,从饮食中吸收的胆固醇不能被肝脏吸收,滞留在乳糜微粒残体中,也会严重增加动脉粥样硬化。现在流行的生酮飲食(ketogenic diet),可能对减肥和降血糖都非常有效,但一个让人担心的风险是会升高胆固醇,特别是对那些有胆固醇代谢基因缺陷的人。正在实践生酮饮食的人应该跟踪一下自已的血脂,任何造成胆固醇升高的饮食都可能是减寿的,只是胆固醇升高动脉粥样硬化推进的坏处一时感觉不出来。低脂与高碳水饮食是美国心脏协会二十年前推荐的降胆固醇饮食,降胆固醇确实有效,但是这个饮食方案的副作用也显而易见,容易肥胖和二型糖尿病随之增加。从一项临床营养学实验的结果看,低脂饮食,中等度不饱合脂肪酸饮食,和用牛油果(150g)替代部分不饱合脂肪酸的饮食等三种治疗饮食(therapeutic diet)相比于普通的饮食(control diet)都能让LDL-C下降20%,其中牛油果饮食不仅让LDL-C下降的程度更大,而且是唯一的饮食同时也降低LDL颗粒数目。低脂饮食虽然降胆固醇的程度差不多,但LDL颗粒数目有所增加,说明肝脏分泌VLDL数量增加。这个临床实验说明,低脂高碳水饮食并不是最佳方案,中等量不饱和脂肪酸加上大量植物固醇(plant sterols)是比较好的方案。植物固醇是植物中类似胆固醇的成份,在肠道中可以阻止胆固醇吸收。植物固醇高的食品包括牛油果,各种坚果豆类和芝麻油。有很少的人会有ABCG5/ABCG8基因缺陷,这些人不能吃植物固醇。另外高纤维食品能阻止胆固醇和油脂吸收降低胆固醇,最常吃的包括燕麦和各种全谷物食品。
消除氧化自由基
吸烟会直接增加血液中氧化自由基,增加对血管壁内膜的损伤。对于某些有SOD3基因缺陷的人,吸烟的危害会更大。
氧化自由基的问题很大,LDL脂蛋白微粒会被氧化自由基氧化成为ox-LDL。氧化过程可以发生在血液循环中,但更多发生在滞留于血管壁夹层中的脂蛋白微粒上。ox-LDL会吸引免疫细胞进入血管壁夹层前来吞食ox-LDL,引发局部炎症反应,同时形成泡沫样细胞,迈向动脉粥样硬化的里程碑。血管壁夹层中的氧化自由基来源于周围内皮细胞呼吸链泄漏的氧化自由基,可能也有炎症反应时免疫细胞释放出来的氧化自由基。由于LDL是油脂分子,主要依靠LDL上的脂溶性维生素E抵挡氧化自由基。流行病学的研究发现摄入维生素E多的人患心血管病的风险降低。但是一个分子的维生素E只能抵挡一个分子的氧化自由基,被氧化了的维生素E在体内需要维生素C将它还原再生,才能被反复使用,所以保持强大的维生素C也很重要。维生素E和维生素C属于可再生抗氧化剂,在体内可以被身体自带的强大还原系统源源不断的还原再生,重复使用。身体自带的抗氧化化系统通过戊糖磷酸化途径不断的分解葡萄糖产生还原剂NADPH, 再通过NADPH还原再生谷胱甘肽,再通过谷胱甘肽还原再生维生素C,通过维生素C还原再生维生素E。维生素E最好从食物摄入,不建议维生素E营养补充剂,因为市面上的维生素E营养补充剂是合成的dl-alpha-tocopherol,只有1/8的成份是正确生物构象,其他7/8的成份虽然也能中和氧化自由基但是可能不能在体内被维生素C还原再生。目前为止所有使用维生素E补充剂的临床实验都不能降低心血管病风险,而且几乎一致的是增加各种病因的死亡率。天然维生素E的最好来源是各种种子和坚果,含量最高的是小麦胚芽油(wheat germ oil)和葵花籽油。维生素E严重缺乏的一个症状是男性不育,维生素E对精子起抗自由基保护作用。在植物中维生素E也是主要存在于芽胚和种子中。除了维生素E脂溶性抗氧化剂,还有很多植物来源的脂溶性抗氧化剂包括胡萝卜素和原花青素等多酚化合物,这些抗氧化剂大量摄入时有一定的抗氧化作用,但是这些分子不像维生素E可以通过维生素C还原而与身体中的强大抗氧化系统衍接,这些分子与氧化自由基一对一反应后就失去抗氧能力,不能被还原再生。
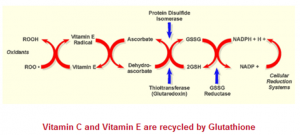
图3. 维生素C和维生素E在体内被谷胱甘肽及NADPH系统还原再生.
加強胆固醇反转运通道活性
胆固醇反转运是身体中清扫多余和损坏胆固醇的通道,加強反转运通道活性可能也可以减缓动脉粥样硬化,不过还没有一个药物在这条通道上取得成功。胆固醇反转运通道的活性与血液中高密度胆固醇HDL-C有关,一般而言这个通道活性增加HDL-C升高,但是简单的通过阻碍胆固醇反转运来提高HDL-C是适得其反,比如通过抑制CETP提高HDL-C。这个通道上两个最重要的基因APOA1和ABCA1的表达水平可以分别被雌激素和维生素A调节。APOA1编码合成的apoA1是组成HDL微粒的核心脂蛋白,HDL就像收集胆固醇费品的小车,从肝脏出发随血液循环去到身体各组织器官收集多余和受损的胆固醇,然后运回肝脏再利用或消毁。动脉粥样硬化病灶里的胆固醇也靠HDL来清除。APOA1基因的表达部分受雌激素调节,这也是为什么女性的HDL-C水平较高(平均在60mg/mL),比男性平均高20%(男性平均在50mg/dL);绝经期后女性的HDL-C水平会下降,下降大概20%到男性相当的水平。这个现象部份解释了女性发生心脑血管病的年龄比男性晚5-10年,同时寿命也平均比男性长大约五年。黄豆和其他豆类食品含有大量异黄酮(isoflavons),又称为植物雌激素,雄性马大量摄入异黄酮后确实会生育力下降,异黄酮营养补充剂能帮助有些人改善更年期综合症症状。经常吃豆腐喝豆浆可能也能增高APOA1基因的表达,从而会对胆固醇反转运有一定的帮助。
胆固醇反转运通道上的另外一个重要基因ABCA1负责将细胞中多余的胆固醇泵出细胞传递到HDL上运走,血管壁中沉积的胆固醇也是依靠免疫巨噬膜上的ABCA1泵出来由HDL运送回肝脏消毁。ABCA1基因的表达主要受维生素A调节,在高胆固醇血症的动物模型中发现,高表达ABCA1不能减少动脉粥样硬化斑块的数量,但是会减小斑块的大小。这说明ABCA1不能影响粥样硬化的起始,但是能够减缓粥样硬化的发展和恶化。在基因关联性研究发现,负责降解维生素A的CYP26A1基因的一个活性增强变异,会造成体内活化维生素A的浓低,携带这个变异的人在年龄,性别和胆固醇浓度相当的条件下,动脉粥样硬化的斑块比没有这个变异的人明显增大,再次证明ABCA1受维生素A调节,增加ABCA1的表达可以减小动脉粥样硬化斑块的大小。更进一步的动物实验还发现,给小鼠喂食胡萝卜素也会使动脉粥样斑块缩小,但是小鼠模壁同时删除BCO1基因后,胡萝卜素的保护作用也就消失了。胡萝卜素是维生素A的前体,在体内需要经过BCO1基因编码的酶转化后成为视黄醇(retinol)才有生物活性,删除BCO1基因后胡萝卜素失去保护作用进一步说明保护作用是通过维生素A增加ABCA1基因表达实现的。胡萝卜素在绿叶蔬菜红萝卜红薯南瓜中很丰富,但是红胡萝卜素是脂溶性分子,必须和油脂混合在一起才能被吸收。啃新鲜红萝卜几乎吸收不到什么胡萝卜素,白水煮青菜也很难获得胡萝卜素,对于维生素A胡萝卜素来说在肉汤油汤中煮熟煮烂会增加40倍的吸收。人群中有不少一部分人携带BCO1基因的变异,这些人转化胡萝卜素成为视黄醇的能力有限,最好直接摄入动物来源的维生素A(视黄醇)。蛋黄,猪肝,鱼肝油和全脂牛奶含有丰富的活性维生素A视黃醇,在美国超巿里卖的牛奶豆浆和其他代奶制品都添加过视黄醇,但是家里自制的豆浆是缺乏视黄醇的。
这里可以看到,豆腐青菜红薯等看似又便宜又大量的家常食品,在减缓动脉粥样硬化的功能上,包含着深刻的分子生物学原理。
适度运动但避免过度运动
动脉血管壁上的物理损伤是动脉粥样硬化的起始,那么我们不禁会问体育锻练时心跳加快,血流加快速,血压升高,是不是也会增加对血管壁的损伤,促进动脉粥样硬化的形成?流行病学的研究结果显示,适当体育锻练可以降低心血管疾病风险。那么高強度体育运动是增加还是减少心血管疾病风险呢?有研究显示,在马拉松运动员中,如果有家族性高胆固醇血症,这些运动员的动脉粥样硬化会更显著。但是如果发生心肌梗塞,运动员比非运动员死亡率低。究其原因是长期锻练的过程中,因为动脉狭窄造成的心肌供养不足会促使补尝性小动脉血管增生,当冠状动脉堵塞时,增生的小血管会承担部份供血供氧,降低心肌缺血猝死风险。一项称为测量运动员心血管疾病风险(Measuring Athlete's Risk of Cardiovascular events (MARC))的研究釆用CT扫描评估中年运动员冠状动脉硬化程度,包括CT扫描检测钙化斑块和冠状动脉造影。这项研究有284名运动员参加,结果显示运动员比非运动员的血管壁上有更多动脉粥样硬化钙化斑块,男运动员比女运动员有更多钙化斑块,钙化程度和数量随运动员一身运动总量(life long excise volume )的增加而增加。比较不同种类的运动,骑自行车的运动员动脉钙化程度最低,跑步运动员动脉钙化程度最高,其他种类的运动员在这两者之间。虽然动脉钙化一定是动脉粥样硬化病变,但是这些运动员并没有发生急性心肌梗塞,说明运动员的钙化斑块比较稳定,不容易破裂。这项研究也显示运动员身上的动脉硬化斑块比较简单干净,沒有太多油脂沉积和炎症。
作者认为,如果你有家族性高胆固醇血症,或者Lp(a)特别高,这两样都会大大加速胆固醇在动脉血管壁破损处的贴附,加速动脉粥硬化的进程。长期并且高强度体育锻练对这部份人可能是弊大于利。这部份人建议极积就医寻求降低胆固醇和高血压治疗,保持适度但避免高強度体育锻练,坚持每年体检,警惕心血管病症兆。

图4. 分子营养学减缓动脉粥样硬化
以上内容可以总结为简单的几点:
1. 避免高血压,如果靠食品和运动调节不够,就需要吃药。
2. 降低胆固醇,如果光靠食品不够就需要吃药。
3. 戒烟,不过度饮酒,享受生活保持心情舒畅。
4. 摄入充分的新鲜瓜果疏菜,外加小量的坚果以获取充足的抗氧化剂维生素C和维生素E。多吃豆腐青菜红薯南瓜五谷杂粮,少吃大油大肉;鸡蛋牛奶和鱼可以天天有, 补充一点omega-3。
5. 适当锻练但避免过度锻练,特别是胆固醇特别高的人。
6. 阿斯匹林是预防急性心肌梗塞最有效的,但是对于Lp(a)特别低的人,长期服用要考虑脑溢血风险。
降胆固醇药物的工作原理
他汀类降胆固醇药物从八十年代开始推广和普及,是近三十年人类平均寿命显著增长的最主要原因。他汀类药物的作用机制是通过抑制内源性胆固醇合成通道上的限速酶,HMG-CoA 还原酶,降低细胞内胆固醇合成,致使细胞内部胆固醇浓度下降。我们在第二章讲过肝脏负责身体中所需胆固醇的合成和调度分配,肝细胞内有一套精密的生物反馈系统来监测和决定是否开啟胆固醇自主合成,是否增加回收血液循环中的胆固醇。这套反馈系统依赖细胞内胆固醇的浓度为开关,当细胞内胆固醇浓度变低,胆固醇感应蛋白就会被激活,相反就会被抑制。当他汀类药物抑制了肝细胞内的胆固醇合成,细胞内部的胆固醇浓度降低,胆固醇感应蛋白激活,进入到细胞核启动一系列基因表达,从而反馈性刺激细胞膜表面低密度脂蛋白受体LDLR数量增加,从而增加肝脏从血液中回收低密度脂蛋LDL,结果LDL-C浓度下降。
他汀类药物是效果最好价格最便宜的降胆固醇药物,对大多数人来说安全性也非常好。但他汀类药物对那些携带有LDLR基因双突变的人没有效果。因为他汀类药实际上是靠增加细胞膜上LDLR的数量来达到降低胆固醇疗效,如果两条染色体上的LDLR基因都突变失活了,增加数量也没有用。另外,他汀类药物不能降低Lp(a)的那部份LDL-C。我们在第四章详细讲过Lp(a),它比普通的LDL更坏。因为Lp(a)的清除主要不是通过肝细胞膜上的LDLR,所以他汀类药对降低Lp(a)无效。如果一个人Lp(a)很高,服用他汀类药物后可以降低由普通LDL运载的那部份胆固醇,但是由Lp(a)运载的那部份胆固醇就下不去了。现在Lp(a) 高还没有药物可以治疗,也不受饮食和锻练影响,对于Lp(a)特别高的病人,现在唯一的治疗方法是体外脱脂法,但这个治疗很麻烦很贵,运用得很少。可以看出降Lp(a)是一个很大并且尚未满足的需求,治药公司也没闲着,已有好几家公司正在开发RNAi药物。脂蛋白a是肝脏合成的蛋白质,应该说特别适合作为RNAi药物的靶点。
有一部份人对他汀类药物不耐受,最主要的问题是肌肉疼痛。造成肌肉疼痛的原因有多种,最常见的一类是药物进入肝脏受阻,造成血药浓度太高;另一类是线粒体不能用长链脂肪酸为燃料,肌肉本身容易疲劳。SLCO1B1基因上的某些变异是造成肌肉疼的最常见原因。SLCO1B1基因编码一个细胞膜上的分子转运泵(solute carrier organic anion transporter),这个泵负责将血液中的他汀类药物转运进入肝脏。肝脏既是他汀类药的靶向组织,也是代谢降解药物的组织。SLCO1B1基因变异失活结果导致他汀类药物在血液中的半衰期增长,血液中statin浓度过高,进入肌肉细胞造成肌肉毒性。大约有15-20%的人服用标准剂量的他汀类药物会出现不同程度的肌肉疼痛。SLCO1B1 gene, c.521T>C是最常见的会导致肌肉疼痛的变导,20%亚洲人有这个变异。携带SLCO1B1变异的人,可以降低他汀类药物的起始剂量,然后逐步升高剂量以寻求达肌肉能够忍受的可降低胆固醇的最佳剂量,但不应该放弃用药。另外,也可以选择耐受性较好的他汀类药物,比如普伐他汀(fluvastatin)肌肉疼痛较少,而辛伐(simvastatin)降胆固醇效果最好,但是更容易发生肌肉痛。另外,可以考虑非他汀类降胆固醇药依泽替米贝(Ezetinibe)和饮食辅助降胆固醇。一些会加重他汀类药物肌肉疼痛的基因与氧化长链脂肪酸有关,包括CPT2和CPT1A ,这些基因上的某些变异会造成肌肉细胞不能很好的燃烧脂肪作为能量,在禁食或长时间运动的情况下,肌肉细胞中葡萄糖耗尽,但又不能用脂肪作为能量,再加上他汀类药物对肌肉的毒性,很容易发生肌肉疼痛。由于CPT2基因变异造成的肌肉疼痛可以通过多吃是碳水化合物,避免禁食,缩短每次运动的时间,运动前喝一点含糖饮料等方法来减轻肌肉症状。
最近几年新出来的降胆固醇神药应该算PCSK9抑制剂(PCSK9 inhibitors)。有两种类型的PCSK9抑制剂,一类是抗体,另一类是RNA干扰。两种类型的PCSK9抑制剂都有很好的降胆固醇效果,对那些心血管疾病风险很高并且已经使用了最大剂量他汀类药物但胆固醇仍不理想的病人,PCSK9抑制剂是最好的选择,唯一的副作用是胆固醇有时降得太低了,增加二型糖尿病风险。PCSK9的抑制剂的另外一个好处是不会引起肌肉疼痛,对那些心血管疾病风险很高,但又不能服用高剂量他汀类药物的病人,PCSK9抑制剂就是必须的选择。PCSK9抑剂最大的问题是价钱非常昂贵,需要约$15,000一年,而他汀类仅仅几百块。所以多数医疗保险不支付PCSK9抑制剂在普通高胆固醇病人身上使用。除了价钱问题,PCSK9抑制不像他汀类药可以口服,需要每两到四周注射一次。最新出来的RNAi更方便些,可以每6个月注射一次。
PCSK9抑制剂靠增加肝细胞膜上的LDLR受体的数量增快回收血液中LDL微粒,使LDL-C下降。大家可能已经注意到了PCSK9是会造成家族性高胆固醇血症的基因之一,造成高胆固醇的突变是活性增加的突变(gain of function),相反PCSK9失去活性的突变(loss of function)则会造成家族性低胆固醇血症。正是因为在人群中观察到有些人PCSK9基因完全失活,但这些人除了血液中胆固醇特别低以外活得很健康。受这一观察的啟发因此发明了PCSK9抑制剂用于降胆固醇。PCSK9参与LDLR的循环使用, 当PCSK9活性增加,内吞进入细胞的LDLR会更多的被消化掉,不能再循环回到细胞膜表面继续使用,相反,当PCSK9活性被抑制,LDLR不会在细胞内被消化掉,而是更多的循环回到细胞膜表面继续参与回收血液中的LDL微粒,从而使LDL-C降低。
他汀类和PCSK9抑制剂都是通过增加肝细胞表面LDLR的数量,从而增加肝脏对胆固醇的回收来达到降低血液中胆固醇的功效。另外一类降胆固醇药物是通过阻碍胆固醇从肠道吸收, 最常用的是默克公司的依泽替米贝(Ezetinibe),其作用机理為阻断Niemann-Pick C1-like 1 (NPC1L1)蛋白质,藉此抑制小肠吸收胆固醇。临床上可以用於对他汀类药物不耐受患者,或者与他汀类联合使用进一步降低胆固醇。
除了直接降低胆固醇的药物外,最近出来的ANGPTL3抑制剂可以同时降低甘油三酯和胆固醇,改善心血管病风险。

结语
随着科学的进步和对基因-疾病的深入认识,分子营养学的原理可以整合到数字化的生活中,在不知不觉中达到最佳的疾病预防效果。这一天可能离我们并不遥远。
从基因的角度解析心血管疾病风险
(一)从肝脏到心脏
(二)细说胆固醇
(三)没人能逃避的动脉粥样硬化
(四)遗传组合
(五)精准医学与营养学
参考文献:
1. Jacobson TA, Ito MK, Maki KC, et al. National lipid association recommendations for patient-centered management of dyslipidemia: part 1—full report. J Clin Lipidol. 2015;9(2):129-169.
2. Jacobson TA, Maki KC, Orringer CE, et al. National Lipid Association Recommendations for Patient-Centered Management of Dyslipidemia: Part 2 [published correction appears in J Clin Lipidol. 2016 Jan-Feb;10(1):211.
3. Grundy SM, Stone NJ, Bailey AL, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/AphA/ASPC/NLA/PCNA Guideline on the Management of Blood Cholesterol: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines [published correction appears in J Am Coll Cardiol. 2019 Jun 25;73(24):3237-3241]. J Am Coll Cardiol. 2019;73(24):e285-e350.
4. Evert AB, Boucher JL, Cypress M, et al. Nutrition therapy recommendations for the management of adults with diabetes. Diabetes Care. 2014;37 Suppl 1:S120-S143.
5. Gidding SS. Special Commentary: Is diet management helpful in familial hypercholesterolemia?. Curr Opin Clin Nutr Metab Care. 2019;22(2):135-140.
6. Catapano AL, Graham I, De Backer G, et al. 2016 ESC/EAS guidelines for the management of dyslipidaemias. Eur Heart 2016;37:2999-3058.
7. Aung T, Halsey J, Kromhout D, et al. Associations of omega-3 fatty acid supplement use with cardiovascular disease risks: meta-analysis of 10 trials involving 77,917 individuals. JAMA Cardiol 2018;3:225-34.
8. Manson JE, Cook NR, Lee IM, et al. Marine n-3 fatty acids and prevention of cardiovascular disease and cancer. N Engl J Med 2019;380:23-32.
9. Appel LJ, Frohlich ED, Hall JE, et al. The importance of population-wide sodium reduction as a means to prevent cardiovascular disease and stroke: a call to action from the American Heart Association. Circulation. 2011;123(10):1138-1143.
10. Franceschini N, Chasman DI, Cooper-DeHoff RM, Arnett DK. Genetics, ancestry, and hypertension: implications for targeted antihypertensive therapies. Curr Hypertens Rep. 2014 Aug;16(8):461.
11. Hermansen K, Dinesen B, Hoie LH et al,. Effects of soy and other natural products on LDL:HDL ratio and other lipid parameters: a literature review. Adv Ther. Jan-Feb 2003;20(1):50-78. PMID: 12772818.
12. Sultan N, Nawaz M, Sultan A, et al. Effect of menopause on serum HDL-cholesterol level. J Ayub Med Coll Abbottabad. Jul-Sep 2003;15(3):24-6. PMID: 14727334. (There was a significant (p < 0.01) decrease in the HDL-C level of the postmenopausal women (46.72 +/- 1.009) as compared with premenopausal women (63.68 +/- 1.78).)
13. Effect of a Moderate Fat Diet With and Without Avocados on Lipoprotein Particle Number, Size and Subclasses in Overweight and Obese Adults: A Randomized, Controlled Trial. J Am Heart Assoc. 2015 Jan 7;4(1):e001355. PMID: 25567051.
14. J W Anderson JW, Johnstone BM, Cook-Newell ME. Meta-analysis of the effects of soy protein intake on serum lipids. N Engl J Med. 1995 Aug 3;333(5):276-82. PMID: 7596371.
15. Reboul E, Trompier D, Moussa M, et al. ATP-binding cassette transporter A1 is significantly involved in the intestinal absorption of alpha- and gamma-tocopherol but not in that of retinyl palmitate in mice. Am J Clin Nutr. 2009 Jan;89(1):177-84. PMID: 19056557.
16. Shaish A, Daugherty A, Schonfeld G, and Heinecke JW. Beta-carotene inhibits atherosclerosis in hypercholesterolemic rabbits. J Clin Invest. 1995 Oct; 96(4): 2075–2082. PMID: 7560102.
17. Zhou F, Wu X, and Amengual J. β-Carotene conversion to vitamin A delays atherosclerosis progression by decreasing hepatic lipid secretion in mice. J Lipid Res. 2020 Nov;61(11):1491-1503. PMID: 32963037.
18. Romaine SP, Bailey KM, Hall AS, Balmforth AJ. The influence of SLCO1B1 (OATP1B1) gene polymorphisms on response to statin therapy. Pharmacogenomics J. 2010 Feb;10(1):1-11. PMID: 19884908.
19. Saeed A, Hadley TD, Jia X, Ballantyne CM. Statin use in carnitine palmitoyltransferase II deficiency. J Clin Lipidol. 2019 May 10. pii: S1933-2874(19)30176-X. PMID: 31235404
20. Chowdhury R, Khan H, Heydon E, et al. Adherence to cardiovascular therapy: a meta-analysis of prevalence and clinical consequences. Eur Heart J. 2013 Oct;34(38):2940-8. PMID: 23907142
21. Serban MC, Colantonio LD, Manthripragada AD, et al. Statin Intolerance and Risk of Coronary Heart Events and All-Cause Mortality Following Myocardial Infarction. J Am Coll Cardiol. 2017 Mar 21;69(11):1386-1395. PMID: 28302290.
美中药源原创文章,转载注明出处并添加超链接,商业用途需经书面授权。
★更多深度解析访问《美中药源》~
★ 请关注《美中药源》微信公众号 ★



















 微信号:美中药源
微信号:美中药源