美国FDA批准强生丙肝药Olysio(simeprevir)上市,市场前景不容乐观
作者:吕顺
【新闻背景】2013年11月22日,美国FDA批准了强生的Olysio(通用名:simeprevir,曾用名:TMC435)上市,用于和聚乙二醇干扰素α和利巴韦林联用,治疗基因I型的慢性丙型肝炎病毒感染。本品为胶囊制剂,每天口服150毫克一次,用于代偿性肝病(患者的肝脏仍能工作),包括肝硬化以及从未接受过治疗或以前接受聚乙二醇干扰素α或利巴韦林治疗但没有效果的成人患者。Medivir因此收到强生1千万欧元的里程金。但是FDA要求强生提供包括种族、是否HIV感染以及其他特定患者群的上市后随访结果。
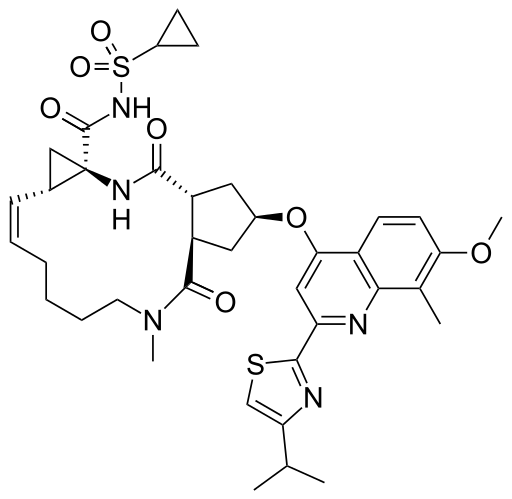
【药源解析】Simeprevir是由Medivir AB研发的一种NS3/4A蛋白酶抑制剂,随后被强生旗下的Janssen爱尔兰收购。Simeprevir的化学结构如下:
Simeprevir是第三个上市的NS3/4A蛋白酶抑制剂。其它两个是默克的Victrelis (boceprevir,博赛泼维)和Vertex的Incivek (telaprevir,特拉泼维),分别在2011年获批上市。和其它两款蛋白酶抑制剂一样,Simeprevir只适用于HCV 基因1型感染,需要与聚乙二醇干扰素、利巴韦林联用。除了以上批准的和聚乙二醇干扰素α以及利巴韦林联用以外,simeprevir还在进行多种临床实验,评价包括治疗基因IV慢性丙型肝炎病毒以及其它联合用药的疗效和安全性。
美国FDA对simeprevir的审批主要基于五个积极的随机、双盲、安慰剂对照的,共注册有两千余患者的晚期临床结果:对于既往未接受治疗的HCV 基因I型感染患者,simeprevir和聚乙二醇干扰素α以及利巴韦林组与安慰剂和聚乙二醇干扰素α以及利巴韦林组的12周持续病毒学应答率(SVR12)分别为80%和50%;对于既往干扰素治疗复发的HCV 基因I型感染患者,simeprevir和聚乙二醇干扰素α以及利巴韦林组与安慰剂和聚乙二醇干扰素α以及利巴韦林组组的SVR12应答率分别为79%和37%。Simeprevir在这些临床实验中有4例患者死亡,但被认定与治疗无关,另外有0.4%的患者有严重不良反应(1例患者重性抑郁,2例患者有光敏反应),这被认定与使用simeprevir有关。
众所周知,丙型肝炎是一种病毒性感染,它引起可导致肝功能减退或衰竭的肝脏炎症。多数感染丙型肝炎病毒者起初没有症状,直至肝功能损害明显,这个过程可能长达几年时间。这些人大多之后变成慢性丙型肝炎,多年后某些患者出现疤痕和肝硬化,还可能导致一系列如出血、黄疸、腹水、感染或肝癌等并发症。根据疾病预防和控制中心统计,大约有320万美国人感染丙型肝炎病毒。以上三个NS3/4A蛋白酶抑制剂的上市,使得HCV基因1型感染的治疗有了三联疗法,即将这三种蛋白酶抑制剂的其中一种与聚乙二醇干扰素和利巴韦林联合应用。这些三联疗法的应答率和聚乙二醇干扰素以及利巴韦林方案相比有效地提高了患者的持续病毒学应答率,但它们也有额外的副作用,除此之外治疗也相当复杂,还有许多药物相互作用的潜在问题。而且到目前为止也未被批准用于除了基因1型以外的其他基因型HCV感染患者。尽管如此,本站路人丙已经详细讨论过Incivek在2011年5月上市以后,当年第四季度销售即达到4.5亿美元,当年就成为超过10亿美元的重磅药物,是史上销售最快的新药。但是好景不长,其下滑的速度也同样惊人,今年第三季度仅销售8000万美元。
因为NS3/4A蛋白酶抑制剂必须与干扰素联用,尽管在一定程度上提高了疗效,仍然遗留了干扰素的感冒样副作用和注射给药给患者带来的不便。尤其是新型在丙肝病毒的复制机制中起重要作用的NS5B聚合酶抑制剂的开发,给以上三个上市的NS3/4A蛋白酶抑制剂造成了更大的挑战。到目前为止,已经有近二十种的核苷酸和非核苷酸类NS5B抑制剂处于不同阶段的临床实验中,其中吉利德的Sofosbuvir估计下个月就能上市,也是首个实现纯口服的抗丙肝药物,对于HCV 的基因2型和3型感染只需与利巴韦林联用,同时FDA专家小组也支持其联合聚乙二醇干扰素、利巴韦林用于HCV基因1型和4型的病毒感染。
正因为包括吉利德的sofosbuvir、雅培生命的三联剂、以及默克的MK-5172/MK-8742组合等全口服抗丙肝药物即将上市,直接导致了Invicek的惨淡销售。Vertex周四(11月21日)宣布以1.52亿美元将Invicek转让给其销售伙伴杨森,从2014年起将不再享受任何销售提成。Incivek成为史上最昙花一现的重磅药物。由此可见,作为同样是NS3/4A蛋白酶抑制剂,而且临床上并未见突出表现的simeprevir的销售前景不容乐观,要想在百亿美元的抗丙肝市场分得较大份额恐怕有点难。
正如路人丙陈述的那样,Incivek和以往销售的快速下降不同,并非由于意外安全性问题或专利到期,而是因为目前有多个全口服丙肝药物组合会很快上市。事实上Incivek是首创药物,在2011,2012年几乎完胜默克的同类药物Victrelis。即使这样也无法保证长时间盈利因为更好的标准疗法即将出现。从另一个侧面反映了me-too类新药研发不仅要优于现有标准疗法,也必须面对崭新靶点的挑战。尤其是今天的新药研发已经和过去有所不同,崭新机理的出现并没有推动药品销售的扩大,而是在原有的份额中分出一杯羹。
美中药源原创文章,转载注明出处并添加超链接,商业用途需经书面授权。★更多深度解析访问《美中药源》~
★ 请关注《美中药源》微信公众号 ★



















 微信号:美中药源
微信号:美中药源