人脑鼠脑:形似神不似
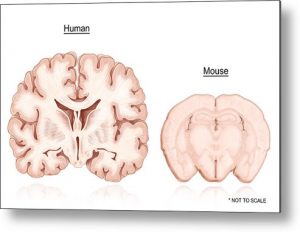
【新闻事件】:这一期的《自然》杂志发表一篇Allen研究所科学家的一项工作,分析人和小鼠大脑的一个叫做中颞回区域的细胞组成。作者用的技术是单细胞细胞核RNA测序,可以根据基因的表达水平大规模分析六层组织中的细胞组成。作者分析了8位供者的15,928个细胞核,其中10,708 为激动型神经元、4,297 为抑制型、923 为非神经元,大概可以分成75大类(24类激动、45类抑制、6类非神经元)。作者用同样方法分析了小鼠类似但不完全相同区域(小鼠用的是整体细胞而不是细胞核),令人意外的是小鼠这个区域的细胞组成与人非常相似,但每类细胞的基因表达水平却相差很大。作者比较14,000个RNA的表达发现其中有10,000个在37类同源细胞中至少一类表达有差别,其中制药工业追逐的主要靶点如离子通道、神经递质受体差异最大。
【药源解析】:尽管根据演化论数据人与小鼠在6500万年前就各奔前程了、但是这么长时间两个物种也没能跳出当初造物主画的圈,说明生命的基本结构高度有序、太大偏差造成的不是物种差异而是生死差异。但是如同两本书虽然远看段落分割差不多但可能讲的是完全不同的故事,人和小鼠除了都爱吃奶酪外相似程度有限。这个研究对中枢系统药物研发有一定意义。新药靶点的发现通常是在基因即DNA水平,但人与小鼠的基因组有97%是相同的。RNA表达和编辑差异可能是造成人鼠物种差异的重要原因之一,与莎士比亚同样词汇量的人不一定都能写出同样水平作品,如何使用这些词汇十分重要。
如果RNA表达、编辑能把类似基因组变成不同物种,把同一物种从健康变成疾病状态应该更容易。另外同类细胞RNA表达水平的空间分布也会影响功能,这个研究发现不同层组织的同类细胞表达水平可能不同、尤其是激动型受体。中枢疾病本来就十分复杂,基因学分析极少能找到主要疾病相关基因。一个可能是多个蛋白需要同时出现异常才能导致疾病状态、也可能是单个受体需要在特定神经突触表达出现微妙异常,无论是哪种情况找到合适的调控药物在现在的技术下都很困难。这可能也是中枢药物成功率如此不堪入目的原因之一。
最令人意外的发现是GPCR、离子通道这类最大家族药靶在这个研究中却显示最大物种差异。根据这个研究GPCR、离子通道本来应该是最不可成药的一类靶点家族,之所以有这样多上市药物(2000年时的统计是50%上市药物是GPCR配体)与它们的发现模式和大量产品为me-too药物有关。历史上多数中枢药物并不是从靶点开始发现的(当然也有prozac这样的例外),而是通过整体动物疗效或临床意外观察发现的。后来的机理研究显示他们是GPCR、离子通道配体可能说明这些膜受体对配体繁杂性(promiscuity)容忍度更高,最容易被当作药靶发现、到底是不是真正作用机理可能各有各的故事。很多动物模型也是先有药物、后有模型,并不能证明模型的预测性和转化能力。相同机理药物可能因为结构类似所以有一定转化成功率,但新机理药物按照氯氮平的发现路径优化多半会被带到沟里。 现在新药发现更依赖理性药物设计,不能因为GPCR配体曾是药物的半壁江山就认为GPCR家族成药性很高。Allen研究所这类研究为制药业敲了警钟,我们要充分利用现代高科技、重新思考中枢靶点的成药性。
美中药源原创文章,转载注明出处并添加超链接,商业用途需经书面授权。★更多深度解析访问《美中药源》~
★ 请关注《美中药源》微信公众号 ★



















 微信号:美中药源
微信号:美中药源