美国FDA批准Adasuve(loxapine)上市,治疗精神分裂症和双相情感障碍
作者:药源
据雅虎美国报道,美国食品药品监管局星期五(12月21日)批准了Adasuve(通用名:loxapine)上市,治疗精神分裂症和双相情感障碍。这个决定是根据FDA精神药物委员会(PDAC)之前的投票结果,专家们以9∶8的投票结果,同意推荐FDA批准Adasuve(洛沙平,loxapine)作为24小时内单剂量鼻腔给药用于存在激越症状的精神分裂症和双相情感障碍患者的治疗。
美国FDA之前批准了Abilify(施贵宝)、Zyprexa(礼来)、和Geodon(辉瑞)三个注射剂用于治疗精神分裂症和双相情感障碍,Adasuve是FDA批准的第一个采用吸入器给药的同类药物。Adasuve使用了Alexza的专利Staccato吸入系统来传递抗兴奋药物洛沙平直接进入肺部,然后进入血液。对于激越症患者而言,吸入剂比注射剂更能让患者接受。吸入之后10分钟起效,本品的安全性和有效性在1600名患者进行的13项临床试验中得到证实。此外,Adasuve口服制剂洛沙平早先已被FDA批准用于精神分裂症的治疗。
之前,FDA专家小组注意到Adasuve的安全隐患,在药物传递到患者肺部整个过程存在潜在副作用。另外今年五月在现场检查其加州Mountain View生产基地时发现不合格设施,拒绝了Alexza的新药申报(NDA)。今年八月,Alexza再次申报了Adasuve的新药申请。
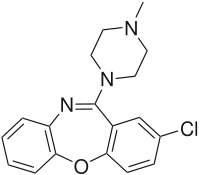
据统计,全美共有240万人罹患精神分裂症和570万人罹患双极性情感障碍。洛沙平的化学结构式如下:
★更多深度解析访问《美中药源》~
★ 请关注《美中药源》微信公众号 ★




















 微信号:美中药源
微信号:美中药源