
继辉瑞Ibrance之后今天FDA批准了第二个CDK4/6抑制剂,诺华的ribociclib,与芳香酶抑制剂联用作为一线用药治疗HR阳性/ HER2阴性绝经后妇女晚期转移乳腺癌
Continue reading …
今天Health Affairs有一篇文章分析美国与西方主要市场药价差异,以及这个差异与研发投入比较的文章。作者统计了2015年生产世界前20个大药的15个药厂的主要产品(>5%总销售)销售情况。结果发现这些产品的美国药价平均比与欧洲、加拿大高40%,相当于1160亿美元的“附加利润”
Continue reading …
今天泰福宣布出资1.6亿现金加9千万美元里程金收购Concert制药的氘代Kalydeco(学名CTP-656),Concert股票上扬62%,市值达到3.5亿美元。
Continue reading …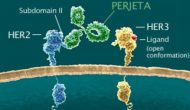
今天罗氏旗下基因泰克宣布其HER2/HER3二聚抑制剂Perjeta在一个叫做Aphinity的三期临床试验中达到一级终点。这个试验比较Perjeta/赫赛汀/化疗组合与赫赛汀/化疗组合控制早期HER2阳性乳腺癌手术后转移复发的疗效。
Continue reading …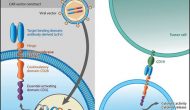
今天Kite公布了其CAR-T药物KTE-C19(Axicabtagene ciloleucel,简称Axi Cel)的6个月数据,这是评价Axi Cel持久性的一个关键数据。
Continue reading …
今天包括辉瑞、赛尔基因在内的若干投资者宣布出资3800万美元成立一个叫做Arrakis的生物技术公司,由制药界大佬Mike Gilman担任CEO。Arrakis将成为第一个系统寻找小分子RNA抑制剂的企业。
Continue reading …
今天美国生物技术公司Trevena宣布其突破性药物、偏爱型阿片受体激动剂oliceridine在两个三期临床达到试验一级终点。在这两个叫做APOLLO-1 和APOLLO-2三期临床中,拇囊外翻和腹壁整形患者手术后使用静脉滴注oliceridine止痛效果显著优于安慰剂,达到试验一级终点。但在关键的二级终点、即比吗啡耐受性的提高Oliceridine表现平常。Oliceridine虽然获得FDA突破性药物地位、并达到试验一级终点,但投资者期待值更高。 Trevena股票今天暴跌40%。
Continue reading …
今天赛尔基因宣布其S1P1调控剂ozanimod在一个叫做SUNBEAM的三期临床试验中比百健的beta干扰素(商品名Avonex)显著降低多发性硬化症患者的复发频率
Continue reading …
昨天FDA批准了Valeant的IL17A受体抗体brodalumab(商品名Siliq),用于中重度银屑病。因为去年外部专家组曾以18比0全票支持Siliq上市,所以昨天的消息并不出人意料。
Continue reading …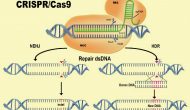
今天美国一个专利纠纷与上诉委员会的三位法官认为Broad的CRISPR 专利没有与伯克利的类似专利抵触,这个所谓“Interference proceeding”(专利抵触程序)结果令张锋暂时成为CRISPR技术的法定发明人
Continue reading …
今天两个开发中枢神经药物的生物技术公司先后公布了两个阳性二期临床结果。Sage Therapeutics的GABA受体激动剂SAGE-217在一个有13位重度抑郁患者参与的临床试验中比安慰剂降低20点汉密尔顿指数、62%的病人完全缓解
Continue reading …
今天《细胞》杂志发表一篇文章号召全世界教授联合起来共同开发、上市低价新药的文章。这篇文章认为现在药价过高是因为药厂过于贪婪、高管工资太高、开发效率低下、竞争无序造成。
Continue reading …
今天FDA批准了Marathon Pharmaceutical的地夫可特(商品名Emflaza)用于5岁以上杜氏营养肌不良症(DMD)患者。地夫可特是一个很老的糖皮质激素,今天批准了片剂和口服液两种剂型。因为DMD是个致命儿童罕见病,Emflaza获得了孤儿药、优先审批、优先审批评审券等特殊待遇。尽管这是一个老药,很多国家都有廉价仿制产品,但Emflaza从未在美国上市,厂家的定价为每年8万9千美元。
Continue reading …
昨天吉利德公布了其2017年销售预测,其中丙肝药物Sovaldi和Harvoni的预测销售为75-90亿美元,低于华尔街预测的115亿美元,结果吉利德股票下跌10%。
Continue reading …






















 微信号:美中药源
微信号:美中药源