
昨天Ionis又坐了一次熟悉的过山车。虽然辉瑞的小分子ATTR药物Tafamidis似乎威胁没有预想的大、令其股票上扬8%,但好景不长下午收盘后FDA拒绝了其旗下Akcea的主打产品之一、
Continue reading …
今天FDA批准了Alnylam的RNAi药物Onpattro (通用名patisiran)用于治疗转甲状腺素蛋白淀粉样变性(hATTR,也称家族性淀粉样多发性神经病变,FAP)引起的神经损伤。
Continue reading …
今天SPARK公布了其A型血友病基因疗法SPK8011的一个一二期临床结果。在这个共有12人参与的试验中SPK8011令A型血友病患者出血事件和需要传统治疗频率降低97%,几乎是治愈。
Continue reading …
今天Zogenix公布了其低剂量氟苯丙胺制剂ZX008在第二个Dravet氏综合征症三期临床结果。这个试验招募87名平均年龄9岁的儿童患者,比较在标准疗法背景上加入0.5毫克/公斤/天ZX008与安慰剂的区别。
Continue reading …
因英国政府拒绝支付福泰囊肿性纤维化(CF)系列药物,其CEO Jeff Leiden今天给英国首相特蕾莎梅写了一封公开信,指责英国政府草菅人命,虽然英国是CF高发区但英国卫生部(NHS)认为无法支持这些昂贵药物。
Continue reading …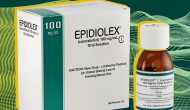
今天FDA批准了GW Pharma的大麻二醇(CBD)液体制剂Epidiolex用于治疗两岁以上儿童的两个罕见癫痫病Lennox-Gastaut 和Dravet 综合征。这是首款成为上市药物的来自大麻的纯化学制剂,专家预计峰值销售可达12亿美元。因为医用大麻在美国很多州已经在使用
Continue reading …
今天Sarepta公布了一个DMD基因疗法的早期临床数据,三位6岁以下儿童患者使用该疗法后肌营养蛋白水平达到正常水平的38%(用另一种定量方法测为正常值的53%),这远超投资者预期的5-10%正常值水平。另一个衡量肌肉健康程度的指标、血液肌酸酐激酶水平比用药前下降87%。
Continue reading …
今天罗氏公布了其双特异抗体、血友病药物Hemlibra (通用名,emicizumab又名ACE910)的两个三期临床结果。在一个叫做HAVEN 3的临床试验中,无VIII号因子抗体患者一周或两周皮下注射一次Hemlibra降低96%和97%的出血事件, ~60%患者一年内没有任何流血事件。
Continue reading …
今天几位华人基因编辑科学家创建的单碱基修复基因编辑公司Beam获得8700万美元A轮支持。Editas的三位创始人MIT的张锋、哈佛的David Liu、和Mass General的Keith Young联手创立了Beam,CEO为Agios的原高管John Evans。
Continue reading …


























 微信号:美中药源
微信号:美中药源