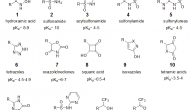
据不完全统计,全球上市的药物分子有超过450个含有羧酸官能团。带有负电荷的羧酸具有水溶性高、生物利用度好等优点,是常见的药效基团(pharmacophore)之一。
Continue reading …
【新闻事件】:福布斯上周发表文章“为何安吉丽娜•朱莉测基因要三千美元?”详细地介绍巨数遗传公司(Myriad Genetics)的BRCA专利案,再次把基因专利的双重影响推到舆论中心。
Continue reading …
5月29日,美国FDA宣布批准葛兰素史克的两个口服新药—Tafinlar(dabrafenib)胶囊和Mekinist(trametinib)片剂,用于晚期(转移性)或无法通过手术摘除的黑色素瘤这种最危险类型的皮肤癌患者。
Continue reading …
国家食品药品监督管理总局(CFDA)正在尝试将中国早期临床试验的通道放开。
记者近日从诺华中国方面确认,该公司治疗肺癌的新药“CMET激酶抑制剂”已经通过了国家食药总局的批准,首次被允许在中国境内开展药物早期临床试验(含一期临床中的一部分),该试验与美国等国家的临床进展同步,产品也有望在全球同步上市。

美中药源同意福布斯评论员Gene Marcial的看法,认为TG Therapeutics是一个值得关注的公司,尤其是其旗下新型抗CD-20单抗ublituximab颇具临床潜力。
Continue reading …
武田制药5月20日发布了旗下一款糖尿病新药Fasiglifam的积极后期临床试验数据。在熊本举行的日本糖尿病学会会议上,武田制药宣布了该药物的一项III期临床试验的数据,数据显示日服一次25mg和50mg剂量的Fasiglifam表现出明显的统计学意义,2型糖尿病患者临床相关的糖化血红蛋白水平降低。
Continue reading …
赛诺菲(Sanofi)和Regeneron制药公司21日宣布,其单抗实验药dupilumab的一个IIa期临床试验取得积极进展,用于治疗中度至重度过敏性哮喘(allergic asthma)。
Continue reading …
制药巨头辉瑞日前(5月20日)宣布终止其ADC实验药inotuzumab ozogamicin的一个关键三期临床实验。这个代号为B1931008的随机、开放标签、双组的临床实验评价inotuzumab ozogamicin对不适合高剂量化疗、复发性或难治性非霍奇金淋巴瘤(non-Hodgkin lymphoma或NHL)患者的安全性及疗效。
Continue reading …
制药巨头辉瑞本周三宣布,其细胞周期蛋白依赖性激酶(CDK)抑制剂palbociclib(PD-0332991)获得美国FDA“突破性药物”称号,这也是美国FDA自2012年7月进一步拓展“创新与安全法案”以来授予的第四个“突破性疗法”,且是唯一一个未上市的实验药获得该项殊荣。
Continue reading …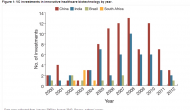
在生命科学创新领域,风险与潜力共存。Nature发文分析了从2000到2012年主要新兴市场生命科学领域的风险投资案例,结果发现,尽管在中国等新兴市场风险投资项目的数量在增加,但生命科学领域创新性风投活动并不多,甚至呈下滑趋势。
Continue reading …
英国国家健康与临床优化研究所(NICE)成立于1999年,是英国最重要的药物研究所之一,负责评估英格兰和威尔士的国民医疗保健制度可以承担哪些药物,并为内科医生制定准则。最近,英国政府宣布,NICE将在制定以药物价值为标准向制药公司支付费用:即“价值基础定价”的计划中担任关键角色。
Continue reading …
年底失去美罗华在欧洲的独家销售权将是罗氏2013年最大的考验。美罗华用于治疗血液肿瘤和类风湿关节炎,其2012年的销售额达67亿瑞士法郎(70亿美元)。此外罗氏还有几个用于治疗癌症和自身免疫性疾病的昂贵生物药的专利权也即将到期,这也为开发低成本仿制药(生物仿制药)的公司提供了一个相当大大的商业机会。
Continue reading …





















 微信号:美中药源
微信号:美中药源